連関資料 :: 実験
資料:320件
-
 血液成分に関する実験
血液成分に関する実験
- 血液成分に関する実験1 <目的> 2匹のラットの血液に含まれる赤血球数、白血球数およびヘモグロビン濃度を測定・比較し、どちらが貧血であるかを予測し、血液成分と病理の関係について学ぶ。 <実験方法> 血球数の測定 ある溶液により希釈した一定量の血液を血球計算盤に採取し顕微鏡下で一定区画中の血球数を測定し、その数より計算して血液1m㎥中の血球数に換算する。 赤血球 操作 血液20㎕を180㎕のハイエム液に入れ10倍希釈し、さらにそれを20㎕取って380㎕のハイエム液に入れ20倍に希釈する。この操作で血液は200倍希釈されたことになる。この希釈血液を被いガラスと血算盤の間に(ニュートン環ができた後
- レポート 農学 ラット 白血球 赤血球
 550 販売中 2007/02/16
550 販売中 2007/02/16- 閲覧(9,425)
-
 錯視実験のレポート
錯視実験のレポート
- 1,目的 錯視とは、視覚による錯覚であり、対象物の大きさや形が実際とは違って知覚されることである。大きさの錯視の代表的なものに、ミュラー・リヤー錯視がある。ミュラー・リヤー錯視とは、実際には斜線の間の線分の長さは同じだが外向きの斜線に挟まれた場合は、内向きの斜線の場合に比べて長く知覚されるというものである。本実験では、ミュラー・リヤーの錯視図を用い、調整法によって錯視量を測定する。 2,方法 <錯視量の定義> 図?では、物理的にはa=bであるのに知覚的にはa<bと見える。もし、逆に知覚的にa=bと見えるように図を描けば、物理的にはa>bとなるであろう。このときの物理的な線分の長さの差、すなわち、a−b=?の値を錯視量と定義する。 <実験手続き> 本実験では、直接?(=錯視量)の値を読み取ることの出来る錯視図計を用いることにする。 被験者は表面を見ながら、図形の左右を手に持って同じ長さに見えるところまで引き伸ばして調節し、実験者は裏面を見て?の値を測る。明らかに短く見える点から徐々に長くして、同じ長さに見えるところまで調整する上昇系列(A)と、逆に明らかに長く見える点から出発して同じ長さに見えるところまで調整する下降系列(D)とがあり、さらに引き伸ばす方向が右(R)からと左(L)からがある。このAとD、RとLの組み合わせ、すなわちAR,AL,DR,DLの4条件についてランダムな順で格4回、計16試行の測定を行う。なお、A,Dいずれの場合にも各試行ごとに、実験者は調整の出発点が一定にならないようにして被験者に手渡す。被験者には自然な態度で図形を観察し、見えるがままの長さを比較して調整するよう、また調整が行きすぎたと思ったら後戻りを繰り返してもよいことを教示する。2,3回練習を行ってから実験を始める。
- レポート ミュラーリヤー 錯視 心理学
 550 販売中 2005/12/13
550 販売中 2005/12/13- 閲覧(49,030)
-
 IC回路の実験
IC回路の実験
- 1 目的 基本的な論理回路をICを用いて構成し、その動作を理解することを目的とする。 2 理論 2.1論理演算 与えられた命題が真(True)であるか偽(False)であるかを、それぞれ1と0に対応させて、命題どうしの論理和(“OR”)、論理積(“AND”)あるいは否定(“NOT”)等を組合せた新命題に対する真、偽の判定を数式化したものが論理式である。以下では、「+」が論理和を、「・」が論理積を、また「 ̄」が否定をあらわすものとする。論理演算では、次の諸式が成立する。 (公理) , , , (交換律) , (結合律) , (分配律) (否定の性質) , , ⇔ かつ (べき等律) , (吸収律) , , (ド・モルガンの定理) , 上記の関係を用いて、複雑な論理式の変形や展開、整理などが可能である。論理式の状態を表示するには、先に示した真理値表のほかに、カルノー図を利用すると便利である 2.2 論理ゲートと論理記号 論理ゲートは論理演算を電子回路的に実現したもので、各種の演算回路がIC化されて用意されている。表1に代表的論理ゲートの論理記号と動作をまとめて示
- 情報 論理 回路 ロック 記憶 目的 対応 内容
 550 販売中 2009/05/21
550 販売中 2009/05/21- 閲覧(3,090)
-
 流体実験レポート
流体実験レポート
- 1.目的 実験による流体抵抗の測定方法を理解し、さらに実際の測定を通して物体まわりの流れと抵抗が発生する理由を理解する。 2.理論 2.1.抵抗係数 流体力は粘性応力によるものと圧力によるものに分解できる。流体抵抗に関して、粘性応力による摩擦抵抗、また圧力による圧力抵抗、あるいは形状抵抗と呼ばれる。つまり、次式のように表すことが出来る。 流体抵抗=摩擦抵抗+圧力抵抗・・・・(1) ある程度レイノルズ数が高ければ、円柱のような鈍い形状の物体に作用する流体抵抗の場合、一般的に圧力抵抗が支配的で、摩擦抵抗は無視できる。 流体抵抗の大きさは無次元化して抵抗係数Cとして表すことが出来る。抵抗係数の定義を次に示す。 ・・・(2) ここで、ρは流体の密度、Uは一様流の流速、Sは一般に対象とする物体を流れ方向にと投影場合の投影面積である。揚力Lにおいても同様に次式の揚力係数Cで表す。 ・・・(3) 2.2.流体抵抗が生じる理由 流れの中に物体をおくと、その物体には必ず流体抵抗が作用することは経験的に分かっていることであるが、ではなぜ流体抵抗が発生するのかその理由について、実在しない非粘性流
- 実験 抵抗 測定 流体 比較 考察 試験 方法 理論 理解
 全体公開 2009/07/25
全体公開 2009/07/25- 閲覧(8,039)
-
 実験(Diels-Alder)
実験(Diels-Alder)
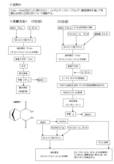
- Diels-Alder反応により得られる2-ノルボルネン-5,6-ジカルボン酸誘導体を通して有機化合物の立体化学について理解する。 <実験方法> (1日目) <目的> 試料1 3.8 g 水 50 ml 100 ml ナス型フラスコ 試料2へ 融点測定 (素焼き板) 加熱還流 15 min (オイルバス&リービッヒ冷却管) 室温で冷却 1 hour 氷冷 吸引濾過 秤量 2.81 g 0.34 gを38班から補う NaHCO3飽和水溶液 10 mlで2回有機層を洗浄する エーテル 20 mlで2回抽出 MgSO4 3.01 gで乾燥 減圧蒸留 (エバポレーター) (2日目) 試料2 2.94
- 有機実験 ディールスアルダー TLC 実験手順 東工大
 550 販売中 2008/04/18
550 販売中 2008/04/18- 閲覧(4,038)
-
 マイクロスリップの実験
マイクロスリップの実験
- マイクロスリップの実験 1.目的 人々は日常の生活の中で、様々な行為を行っている。コーヒーを入れる作業や食事中の手の動きを注意深く観察してみると、対象を掴もうと伸ばした手の動きが、あたかも躊躇したかのように微小に停滞したり、ある対象に向かう手の軌道が途中で別の対象に向かう軌道へと急速に変化したり、ある対象にわずかに接触した後に別の対象に向かうといった微小な行為の修正が頻繁に起こっていることに気づく。このような、いったん開始したにもかかわらず途中で修正されてしまう微小なスリップ様の現象は、マイクロスリップと呼ばれている(Reed,1992;鈴木,2001)。マイクロスリップは、私たちの日常生活での行為について検討する上で非常に興味深い現象である。本実験は、マイクロスリップの起こり方と環境の複雑さとの関連について調べることを目的とする。 2.方法 被験者:単純条件 14名(男4女10)平均19.8才 複雑条件 14名(男5女9)平均19.1才 器具:単純条件では、テーブルに縦4列横3列の枠を書いた紙を敷き、枠内には空の紙コップ2個と砂糖の入ったもの、クリーム粉の入った
- 実験 分析 課題 方法 理解 記録 生活 目的 時間 コーヒー
 550 販売中 2008/08/13
550 販売中 2008/08/13- 閲覧(3,495)
-
 生体制御実験
生体制御実験
- 1.実験目的 1)ヒトの肘関節まわりの筋が発揮している筋張力を,モデルおよび筋電図を用いて推定する. 2)筋疲労によって,1)の方法で推定した筋張力が,関節角度の違い,筋の違いによって,どのように変化するか考察する. 3)筋疲労によって,筋収縮がどのように変化するかについて,周波数解析を用いて考察する. 2.実験装置 今回の実験装置について、以下にシステム構成図を示す。 図2-1 システム構成図 2.1 実験機器 ・NIHON KOHDEN Ag/AgCl電極 ・生体アンプ Multi Channel Amplifier NIHON KOHDEN 型番:MEG/6108M ・オシロスコープ FOUR CHANNEL DIGITAL STORAGE OSCILLOSCOPE Tektronix 型番:TDS2014 ・ひずみアンプ KYOWA STRAIN AMPLIFER 型番:DPM-711B ・ひずみゲージ ・ポテンショメータ ・WE A/D変換ボード YOKOGAWA 形式:WE400 3.実験方法 1)被験者:2名(右利き) 2)筋電図:腕橈骨筋(BR)と上腕二頭筋(BB),上腕三頭筋(TB) 3)運動課題 ・肘関節角度90度における屈曲および伸展の最大随意収縮(Maximum Voluntary Contraction : MVC). ・30%と50%MVCのトルクレベルで等尺性収縮の肘屈曲課題(疲労するまで) ・それぞれ2種類の肘関節角度(30°,90°,完全伸展位=0°)で行う. 4)実験手順 ・おもりを用い,ひずみゲージ(力センサ)の較正値の計測(calibration) ・角度計のcalibration ・EMG電極を筋腹に装着 ・EMGの確認と生体アンプのcalibration ・肘関節角度90°でMVCを数回計測 ・等尺性収縮の屈曲課題 ・モデルのための形態計測+被験者の身体的特性(身長,体重,年齢など)
- レポート 医・薬学 筋疲労 筋電図 上腕二頭筋 上腕三頭筋 腕橈骨筋
 550 販売中 2006/02/01
550 販売中 2006/02/01- 閲覧(2,867)
-
 タンパク質分離実験
タンパク質分離実験
- タンパク質分離実験 実験日 7月6日 目的 ゲルろ過クロマトグラフィーを行い、ブルーデキストリン、ヘモグロビンと2,4-ジニトロフェニルバリンを分離する。 原理 ゲルろ過クロマトグラフィー : 分子ふるいと呼ばれるもので、タンパク質を分子量の大きさにより分画する方法である。樹脂はできスト欄、アガロース、ポリアクリルアミドなどを適当に3次元に架橋して網目構造を持たせたものである。大きなタンパク質分子はゲルの網目構造の中に入ることはできず、小さな分子はゲル内へ拡散していく。ゆえにタンパク質分子が大きいほどゲル内へ進入できない場合が多く、ゲルの外を流れるので速く移動でき、小さいタンパク質ほど内部へ分散されうる頻度が増すので溶出されるのに時間がかかる。この差を利用して、タンパク質を分子量に応じて分画する。 実験材料 溶出液 : 50mM NaCl, 10mM Tris-HCl (pH7.2) 50ml ブルーデキストリン(5mg/ml)、ヘモグロビン(5mg/ml)、2,4-ジニトロフェニルバリン(0.25mg/ml) 混合液 0.5ml 実験方法 カラムの調整 垂直に立てたカラムに溶出液をカ
- 理工学 タンパク質分離 ゲルろ過クロマトグラフィー ブルーデキストリン 4-ジニトロフェニルバリン レポート ヘモグロビン 2
 550 販売中 2006/12/12
550 販売中 2006/12/12- 閲覧(6,902)